Investigadores de
Cataluña han propuesto una nueva vía para combatir las células tumorales
de próstata que se han hecho insensibles a los tratamientos
disponibles. El cáncer de próstata es una enfermedad creciente en todo
el mundo. En Estados Unidos y Europa es uno de los tumores más
frecuentes y figura entre las principales causas de muerte por esta
patología.
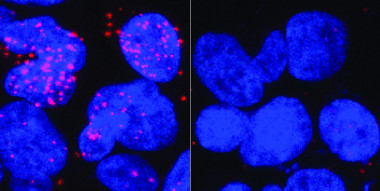
En la
imagen de la izquierda se muestran en rojo las interacciones entre la
proteína receptor de andrógenos (AR) y la proteína TFIIF, nueva diana
terapéutica para el tratamiento del cáncer de próstata avanzado. En la
de la derecha no se registran interacciones, tras eliminar la región del
AR donde se une TFIIF. / Paula Martínez-Cristóbal, IRB Barcelona
En la mayoría de los casos, el cáncer de próstata se cura extirpando
el tumor con cirugía o con radioterapia. Sin embargo, hay un 20% de
pacientes que necesitarán tratamiento para eliminar células tumorales
pero, inevitablemente, deja de funcionar después de dos o tres años y el
cáncer progresa. En este estadio de la enfermedad, ya no hay cura.
Un
equipo liderado por Xavier Salvatella, investigador ICREA en el
Instituto de Investigación Biomédica (IRB Barcelona), ha descubierto un
nuevo frente por donde atacar las células tumorales de próstata que han
desarrollado resistencia al medicamento. El trabajo se publica en la
revista
Structure, y abre nuevas vías terapéuticas contra una enfermedad que provoca, solo en Europa, 75.000
muertes al año.
Las
células tumorales de próstata necesitan que la proteína receptor de
andrógenos esté muy activa para sobrevivir y proliferar. El fármaco que
se usa para eliminar las células tumorales interfiere, de hecho, con
esta proteína. El fármaco actúa uniéndose a una región concreta del
receptor de andrógenos e inhabilita la proteína. "Con el tiempo la
proteína acumula alteraciones, muta, y llega un momento en que es inútil
enviar fármacos a aquella región, porque de hecho, la proteína se
desprende de esa parte", describe.
Para las células tumorales de próstata que han alcanzado el
estadio resistente, esta interacción podría ser su último recurso para
sobrevivir y proliferar
En el
Laboratorio en Biofísica Molecular
dirigido por Salvatella estudian en detalle la estructura
tridimensional y los movimientos atómicos del receptor de andrógenos
para encontrar nuevos puntos de anclaje. Se sabe de hace tiempo que la
proteína tiene una región pequeña, de solo 20 aminoácidos, que es clave
para la supervivencia de las células tumorales.
Ahora, el trabajo describe por primera vez que esta región –habitualmente sin estructura y por tanto
a priori
descartada para enviar fármacos– toma una estructura en forma de
hélice. Al ganar esta hélice –que no se entiende aún cómo se
produce– otra proteína, llamada TFIIF, se engancha. El estudio evidencia
que dicha interacción promueve la actividad del receptor de andrógenos y
aseguraría la supervivencia y multiplicación de las células tumorales.
Encontrar fármacos eficaces
Así,
aparte de la región de 20 aminoácidos que ya antes se conocía como
posible diana terapéutica, el equipo del IRB Barcelona añade la proteína
TFIIF. "El hecho de que sea una proteína plegada con una estructura
mejor definida, hace más fácil buscar fármacos que interfieran con ella.
Creemos que para las células tumorales de próstata que han alcanzado el
estadio resistente, esta interacción podría ser su último recurso para
sobrevivir y proliferar", explica Salvatella.
"Hemos comprobado en células
in vitro
que si eliminamos la región, la proteína TFIIF no se pega al receptor
de andrógenos. Y si la interacción falla, el receptor de andrógenos es
menos funcional, que es lo que se busca", describe Elzbieta Maria Szulc,
estudiante de doctorado "la Caixa" en el IRB Barcelona.
Los
científicos están buscando fármacos que interfieran con TFIIF, en
colaboración con un grupo de expertos en simulaciones computacionales.
“Si después estos fármacos tendrán un efecto beneficioso en células aún
no lo sabemos, pero hay datos que nos hacen ser optimistas", declara
Salvatella.
Referencia bibliográfica:
Eva De Mol,
Elzbieta Szulc, Claudio Di Sanza, Paula Martínez-Cristóbal, Carlos W.
Bertoncini, R. Bryn Fenwick, Marta Frigolé-Vivas, Marianela Masín, Irene
Hunter, Víctor Buzón, Isabelle Brun-Heath, Jesús García, Gianni De
Fabritiis, Eva Estébanez-Perpiñá, Iain J. McEwan, Ángel R. Nebreda, and
Xavier Salvatella. Regulation of androgen receptor activity by transient
interactions of its transactivation domain with general transcription
regulators.
Structure (2017)
https://doi.org/10.1016/j.str.2017.11.007
En
este trabajo han colaborado el laboratorio de Angel R. Nebreda y el
Laboratorio de Bioinformática Experimental, ambos del IRB Barcelona, y
la Universidad de Barcelona. El estudio ha recibido financiación del
Consejo Europeo de Investigación (ERC en sus siglas en inglés), la
Fundación "la Caixa", el programa Marie Curie de la Unión Europea y el
Ministerio de Economía y Competitividad a través de fondos FEDER.

